Để đảm bảo an toàn trong việc sử dụng và phân phối thuốc điều trị COVID-19 Molnupiravir, Sở Y tế TPHCM đã có chỉ đạo khẩn về việc sử dụng, lưu hành loại thuốc này có kiểm soát.
Theo đó, Phó Giám đốc Sở Y tế TPHCM Nguyễn Hoài Nam chỉ đạo Trung tâm y tế các quận huyện, TP.Thủ Đức và các bệnh viện trên địa bàn thành phố tuân thủ đề cương và quản lý thuốc trong chương trình sử dụng thuốc Molnupiravir có kiểm soát.
Các đơn vị tham gia triển khai chương trình cần tuân thủ đề cương nghiên cứu đã được Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia thẩm định, chấp thuận và đã được Bộ Y tế phê duyệt, bảo đảm an toàn tuyệt đối cho bệnh nhân.
Đề cương nghiên cứu đã nêu rõ, tiêu chuẩn lựa chọn bao gồm đối tượng mắc COVID-19 thể nhẹ, trên 18 tuổi, có kết quả xét nghiệm kháng nguyên nhanh hoặc RT-PCR dương tính với SARS-CoV-2, không có các dấu hiệu viêm phổi hoặc thiếu ôxy, nhịp thở 20 lần/phút, SpO2 từ 94% trở lên, có thể dùng thuốc bằng đường uống…
Các đối tượng bị loại trừ bao gồm người bệnh quá mẫn cảm hoặc chống chỉ định với thuốc hoặc bất cứ thành phần nào của thuốc, tiền sử mắc virus viêm gan B hoặc C kèm xơ gan, bệnh gan giai đoạn cuối, ung thư biểu mô tế bào gan, tiền sử viêm tuỵ cấp trong vòng 3 tháng hoặc viêm tuỵ mạn, tổn thương thận cấp, suy thận nặng hoặc phải chạy thận nhân tạo, lọc màng bụng trong quá trình sừ dụng thuốc, phụ nữ có thai, đang cho con bú.

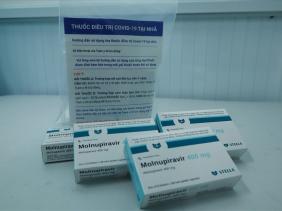
Thuốc Molnupiravir điều trị COVID-19. Ảnh: Nguyễn Ly
Khi sử dụng thuốc, bệnh nhân nam không hiến tinh trùng, quan hệ tình dục phải sử dụng biện pháp tránh thai ít nhất trong 90 ngày đối với nam và 28 ngày với nữ sau liều thuốc cuối cùng. Ưu tiên các đối tượng có ít nhất một yếu tố nguy cơ làm bệnh tiến triển nặng.
Vừa qua, Bộ Y tế cấp phép lưu hành cho 3 thuốc điều trị COVID-19 chứa hoạt chất Molnupiravir hàm lượng 200mg và 400mg, hạn dùng 6 - 8 tháng với giá thành từ 250.000-300.000 đồng/hộp.
Cục Quản lý dược cũng đề nghị các Sở Y tế giao, phối hợp với các cơ sở điều trị theo dõi, giám sát, phát hiện, xử trí các trường hợp gặp phản ứng có hại của thuốc về trung tâm theo dõi phản ứng có hại của thuốc tại Hà Nội hoặc TPHCM, và có trách nhiệm theo dõi, cập nhật và báo cáo về Cục Quản lý dược.
Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc của Bộ Y tế có thông báo không dùng thuốc Molnupiravir cho phụ nữ có thai, trẻ dưới 18 tuổi do có tác dụng phụ, thuốc cũng ảnh hưởng đến tinh trùng của nam giới.
Về giới hạn sử dụng thuốc, hội đồng khuyến cáo Molnupiravir dùng trên bệnh nhân có thời gian khởi phát triệu chứng dưới 5 ngày, không sử dụng quá 5 ngày liên tiếp, không sử dụng để dự phòng sau hay trước phơi nhiễm để phòng COVID-19.
Molnupiravir không được khuyến cáo sử dụng trong thời kỳ mang thai. Phụ nữ chuẩn bị mang thai nên sử dụng biện pháp tránh thai hiệu quả trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng. Dựa trên khả năng xảy ra các phản ứng có hại cho trẻ sơ sinh từ Molnupiravir, không khuyến cáo F0 là phụ nữ nuôi con nhỏ cho con bú trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng.
"Để đảm bảo an toàn, hiệu quả, chỉ sử dụng thuốc Molnupiravir khi có đơn của bác sĩ theo đúng chỉ định, các giới hạn sử dụng và các cảnh báo, thận trọng của thuốc. Không tự ý mua, sử dụng thuốc Molnupiravir trôi nổi, không rõ nguồn gốc, xuất xứ trên thị trường” đại diện Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc của Bộ Y tế nhấn mạnh./.
Nguồn: Nguyễn Ly/laodong.vn


